2022江西紡織服裝周暨江西(贛州)紡織服裝產業博覽會隆重舉行
為深入學習貫徹落實黨的二十大和二十屆一中...
文 | 雷珍怡 海若鏡
編輯 | 海若鏡
每逢過節胖三斤,減肥一直是大眾熱議的話題。2022年,諾和諾德“重磅炸彈”藥物司美格魯肽漲價斷貨、供不應求,全球銷售額高達109億美元,GLP-1靶點藥物在降糖、減肥領域的潛力走紅出圈,相關多肽類藥物的臨床試驗進展也牽動市場神經。
2月6日,禮來宣布:其在研的Tirzepatide(替爾泊肽)用于肥胖或超重成人患者的中國III期臨床試驗,取得積極結果,達到主要終點和所有關鍵次要終點;總體安全性與先前報道相似。盡管還未揭盲,但III期臨床試驗的結果意味著,這款降糖藥距離在中國獲批“減肥”適應癥已不會太遠,有望在今年過評上市。
作為一款GLP-1(胰高血糖素樣肽-1)、GIP(葡萄糖依賴性促胰島素多肽)雙受體激動劑,禮來替爾泊肽2022年4月公布的三期臨床數據顯示,在肥胖癥或超重人群,接受最高劑量(15mg)治療的患者平均體重降低22.5%(約24公斤),其中63%的受試者體重降低至少20%。
眾多Ⅲ期臨床研究中,替爾泊肽是個將體重平均降低超過20%的在研藥物。GLP-1與其他靶點聯合、增強減肥效果的潛力,不容小覷。
據諾和諾德財報顯示,司美格魯肽2022年銷售額達109億美元,超越度拉糖肽的74.4億美元,成為年銷售額破百億美金的GLP-1藥物。
去年開始,司美格魯肽作為“減肥神藥”走紅社交媒體,詢問“能否開降糖藥減肥”的比比皆是,一度導致醫院斷藥。為了優先保障糖尿病患者用藥,多家醫院要求僅內分泌科醫生可對糖尿病人和肥胖癥患者開此處方藥。
目前,司美格魯肽在醫藥電商平臺供應量相對充足,但價格水漲船高。在某互聯網平臺上查詢發現,1.5ml劑量的司美格魯肽售價已漲超700元,同劑量醫院原售價478元;3ml劑量的司美格魯肽的價格約為1100元,同劑量原售價為814元。即便漲價,每周注射一次帶來的立竿見影減肥功效,仍吸引眾多愛美人士以身試藥。
為在FDA獲批減重適應癥,諾和諾德IIIa期臨床曾招募大約4500例超重或肥胖成人患者(BMI≥30或BMI>27且合并一種以上肥胖相關疾病),開展了4項試驗,每項試驗跟蹤時長為68周。數據顯示,司美格魯肽2.4mg劑量治療治療68周,可使非糖尿病受試者體重降低15%-18%。2021年6月,司美格魯肽的肥胖適應癥獲FDA批準,成為可用于體重管理的長效GLP-1受體激動劑。
2022年8月,司美格魯肽用于肥胖適應癥的中國三期臨床試驗完成,盡管臨床研究結果未詳細披露,但其超適應癥用藥已十分常見。其2021年獲批進入中國,2022年諾和泰(司美格魯肽皮下注射劑商品名)在中國銷售額達20.85億元人民幣,可見市場教育速度和接受程度高漲。
時隔半年,肥胖適應癥上,禮來潛力新藥替爾泊肽的中國三期臨床試驗也達到主要終點和所有關鍵次要終點。在禮來替爾泊肽的全球III期臨床研究(SURPASS-2)中,頭對頭與司美格魯肽的臨床效果進行了效果上的比較。
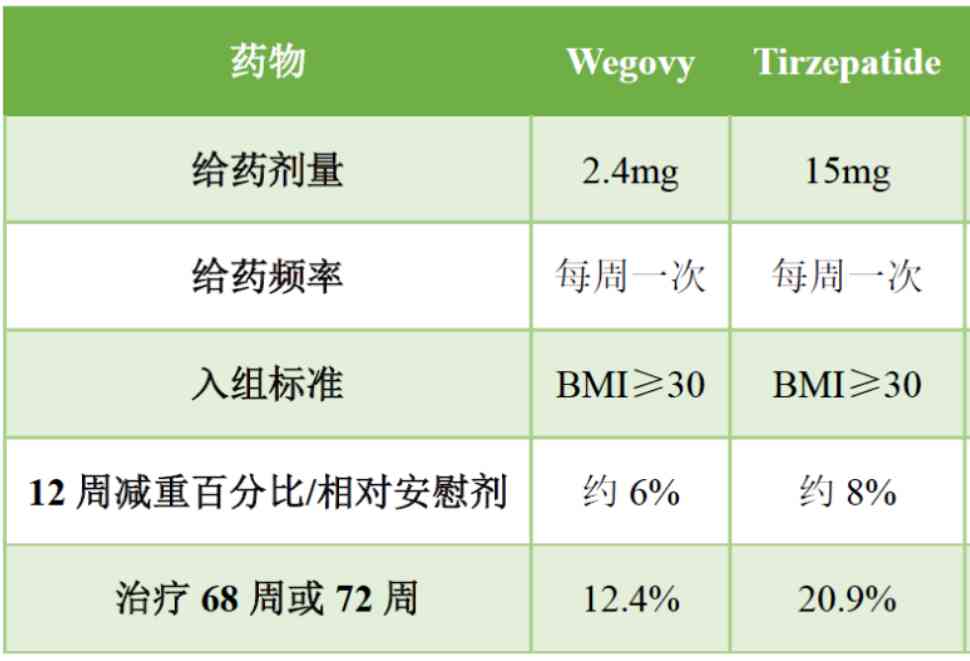
司美格魯肽VS替爾泊肽臨床試驗對比,來源:醫藥筆記
試驗結果顯示,減重方面,替爾泊膚5mg、10mg和15mg劑量下,相較于基線體重(207磅),替爾泊肽受試者平均減重17磅、21磅和25磅;而司美格魯肽(1mg)受試者平均減重為13磅。
在與安慰劑組的對比中,招募了2539例BMI≥30或27、至少有一種肥胖并發癥的成年受試者,等比例隨機使用替爾泊肽5mg、10mg、15mg與安慰劑組。結果顯示,72周時,各組體重分別降低了16.1kg、22.2kg、23.6kg,安慰劑組僅下降2.4kg。其中,15mg組減重超過20%的比例為63%。
替爾泊肽作為GLP-1/GIP雙靶點受體激動劑,降糖適應癥已于2022年5月獲得FDA批準在美國上市,減重適應癥已進入FDA快速通道審批程序。在中國,這款first-in-class藥物的降糖適應癥于2022年9月向NMPA遞交上市申請,一旦獲批進入市場,有望復制司美格魯肽的盛況,同時緩解司美格魯肽供應不足的問題。
早在2014年,FDA批準了諾和諾德的利拉魯肽用于肥胖癥治療,盡管利拉魯肽需要每天注射用藥、依從性受限,但仍顯示出了強大的吸金能力,2020年,減肥版利拉魯肽(Saxenda)銷售額已達8.6億美元,占全球減重藥物銷售額的相當比例。減重效果更好、且只需一周注射一次的司美格魯肽上市后,正在“顛覆”減肥市場。
根據弗若斯特沙利文統計,2016-2020年,全球減肥藥物市場規模由18億美元增長至26億美元;2016-2021年,中國減肥藥市場規模將從2.6億元人民幣增長至30億元,年復合增長率達50.3%。
當前,國內尚未有GLP-1受體激動劑產品獲批肥胖適應癥,國內臨床階段藥物仍以二型糖尿病為主。仿制藥方面,由于利拉魯肽中國專利已到期,國內華東醫藥、江蘇萬邦生化、愛美客等布局了利拉魯肽注射液Saxenda的生物類似藥,其中華東醫藥已提交肥胖適應癥的上市申請。
另外,司美格魯肽的專利保護期至2026年3月,這意味著距離國產仿制藥上市還有三年多,但中美華東、重慶派金申報的司美格魯肽注射液臨床試驗申請已于2022年獲得批準。其中華東醫藥雙線布局利拉魯肽、司美格魯肽生物類似藥,在減肥藥研發領域可謂堅定布局。
在創新藥研發方面,除了替爾泊肽、司美格魯肽超重適應癥的臨床試驗外,國內信達生物、上海仁會、鴻運華寧、恒瑞醫藥的新藥研發較為靠前。
其中,信達生物的GLP-1/GCGR雙重激動劑IBI362,已在國內啟動超重/肥胖適應癥三期臨床試驗,首例受試者給藥已于2022年11月完成。IBI362是信達生物和禮來共同研發的一類新藥,肥胖適應癥上,國內創新藥中研發進展較為靠前。國際上同類減重產品研發序列中,以體型高大的西方高加索人群為主,而IBI362的臨床試驗將尋找大規模、更加具有中國人群代表性的臨床證據。
上海仁會研發的GLP-1受體激動劑貝那魯肽,是國內糖尿病領域個創新藥,2017年上市。其治療肥胖適應癥的臨床試驗,2019年5月即已啟動臨床III期,2021年6月三期臨床434例受試者全部出組。但因半衰期問題,貝那魯肽需每日三次進行皮下注射,患者順應性交叉。
鴻運華寧的原創肥胖癥新藥GMA106,2022年11月在澳洲Ib期臨床研究完成劑量組全部受試者給藥;恒瑞醫藥的諾利糖肽也處于臨床二期階段。
除了下游創新藥、生物類似藥的研發,司美格魯肽等GLP-1的火爆,正帶動上游肽類原料藥和CDMO企業迎來新機遇。司美格魯肽的原料藥生產技術壁壘較高,以往供給也以進口為主;2021年底諾和諾德合作CMO企業的GMP出現問題,一度中斷了美國Wegovy的供應,也導致司美格魯肽的供不應求。
2023年1月,蘇州天吉生物、江蘇諾泰生物兩家藥企注冊申報的司美格魯肽原料藥,已經獲得NMPA受理,一旦獲批,將迎來業績增長新機會。此外,國內藥明康德、凱萊英等CDMO企業也布局了一體化多肽合成平臺,隨著下游新藥研發推進、注冊上市,也將帶動上游肽類原料藥和CDMO企業的發展。
盡管司美格魯肽等GLP-1受體激動劑的安全性、有效性得到了臨床試驗的有力驗證,但對于很多用藥者而言,是“雙重”超適應癥用藥:一方面,當前司美格魯肽等在國內主要適用于二型糖尿病患者,尚未獲批超重/肥胖適應癥;再者,相關臨床試驗多選擇BMI≥30或27的肥胖/超重受試者,而不少臨床用藥者BMI并未進入這一區間,屬于健康人群,僅是出于心理上對“瘦”、“美”的追求選擇減肥。
在不良反應和禁忌人群方面,司美格魯肽最常見的胃腸道不良事件報告率高達84.1%,如惡心、腹瀉、嘔吐和便秘等癥狀。用藥禁忌警告中,包含著“胰腺炎、膽囊問題、低血糖、急性腎損傷、糖尿病視網膜病變、心率加快和自殺行為”,以及“有甲狀腺C細胞腫瘤風險”的黑框警告。
另外,對于體重反彈問題,與其它降壓藥、降糖藥一樣,司美格魯肽等停止用藥后,原本的抑制機制便不復存在,食欲會逐步恢復,體重也可能反彈。信達生物臨床開發副總裁錢鐳講到,“從我看到的文獻來看,(體重)是朝著基線走,但沒有觀察到會超過基線。可能半年到一年會恢復到原基線,當然這也取決于用藥后減肥的程度,如果減了15-20%,那不太容易回到基線;如果只減了5%,可能就很容易恢復。”
臨床醫生出身的錢鐳,也從醫學視角分享道,人變瘦后,下丘腦體重調節中樞可能會呈現再平衡,體內腸道菌群也會發生一定變化;(減肥后)配合飲食運動、生活環境改善,讓機體轉換至新環境中,就比較有希望保持體重。
盡管多肽藥物GLP-1相對安全,但司美格魯肽等均為處方藥、且減肥屬于超適應癥用藥,最為穩妥的方式仍是經由醫生問診檢查,判斷是否適合用藥、使用劑量和用藥爬坡方式等。

為深入學習貫徹落實黨的二十大和二十屆一中...

Burberry是一個具有濃厚英倫風的著...

高奢月子中心圣貝拉(SAINT BELL...

近年來,國際政治經濟環境復雜多變,不確定...

如果有這樣一...

近日上海智美顏和以60后--90后的不同...
名品導購網(www.cctv-ss.com)ICP證號: 蘇ICP備2023000612號-5 網站版權所有:無錫錫游互動網絡科技有限公司
CopyRight 2005-2023 版權所有,未經授權,禁止復制轉載。郵箱:mpdaogou_admin@163.com